Dr. Marc Siegel on AstraZeneca withdrawing COVID-19 vaccine: I am concerned about the delay
Fox News medical analyst Dr. Marc Siegel discusses AstraZeneca withdrawing its COVID-19 vaccine as concerns over side effects grow on 'Special Report.'
A combination COVID-influenza vaccine is apparently one step closer to hitting the market.
Moderna, which is developing the experimental vaccine, announced Monday that in phase 3 clinical trials, mRNA-1083 achieved a better immune response than other vaccines.
The combination vaccine includes mRNA-1010 (Moderna’s vaccine candidate for seasonal influenza) and mRNA-1283 (the company’s "next-generation COVID-19 vaccine candidate"), according to a press release from the company.
"This data serves as a milestone for the industry’s pursuit of a flu and COVID-19 combination vaccine, which could change the way we manage the respiratory illness season," Francesca Ceddia, chief medical affairs officer at Moderna, said in a statement to Fox News Digital.
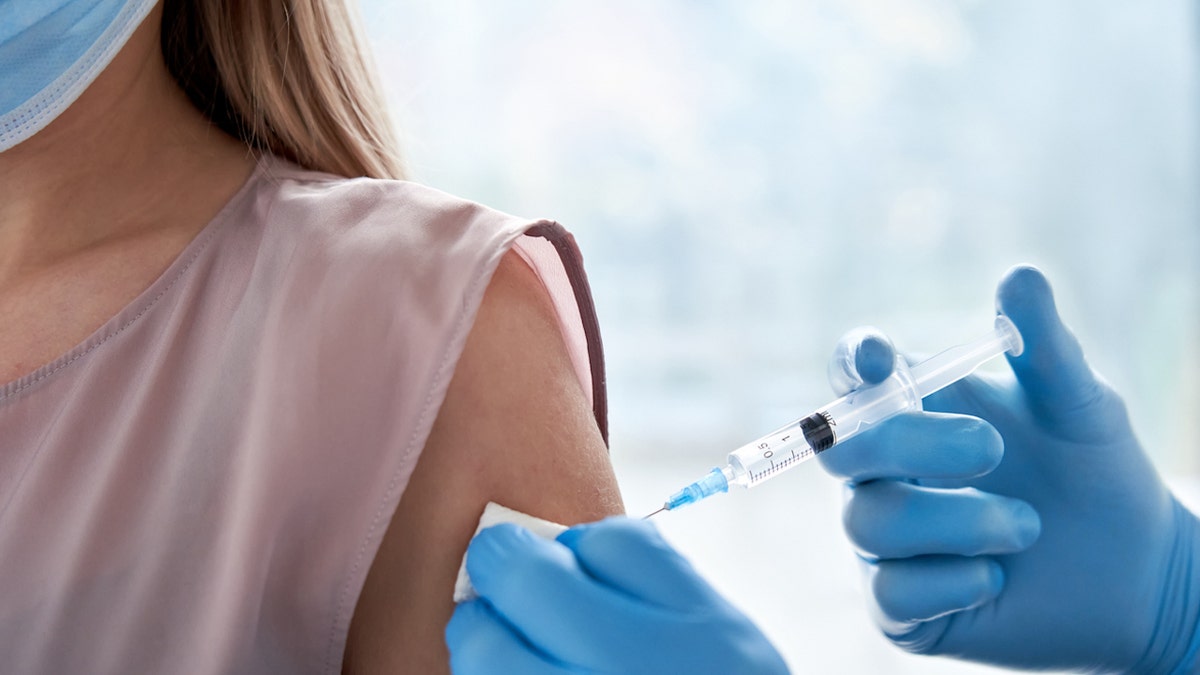
A combination COVID-influenza vaccine is one step closer to hitting the market with this new announcement from Moderna. (iStock)
"With mRNA-1083, we may be able to not only offer the convenience of dual protection in a single shot, but we also may offer enhanced immunity compared to today’s standalone vaccines against the two respiratory diseases with the largest burden on health care systems," she continued.
"Our hope is that with improved convenience comes improved compliance — helping to advance public health and lower rates of severe outcomes related to COVID-19 and flu."
Moderna is the only company with a positive phase 3 flu and COVID combination vaccine, according to the company's press release.
MANY YOUNG KIDS ARE NOT GETTING 'LIFE-SAVING' VACCINES
Moderna’s phase 3 trial was a randomized, double-blinded study that included two independent groups, each consisting of 4,000 adults.
One group included adults age 65 and older, who compared the experimental vaccine to Fluzone HD, an enhanced influenza vaccine, and Spikevax, Moderna's currently licensed COVID-19 vaccine, the release stated.

Moderna announced Monday that in phase 3 clinical trials, mRNA-1083 achieved a better immune response than other vaccines. (REUTERS/Brian Snyder)
The second group, which included adults 50 to 64 years old, compared mRNA-1083 to Fluarix, a standard dose influenza vaccine, and Spikevax.
In both groups, mRNA-1083 resulted in "statistically significantly higher immune responses against three influenza virus strains (H1N1, H3N2, and B/Victoria) and against SARS-CoV-2," according to the release.
"One can never predict rare adverse events."
Florida State Surgeon General Dr. Joseph A. Ladapo, who was not involved in the vaccine trial, shared his reaction in an exclusive statement to Fox News Digital.
"I've made it clear why the mRNA COVID-19 vaccines are not appropriate for human use, and researchers will continue to uncover additional concerns and adverse events caused by these mRNA shots," he said.

Florida State Surgeon General Dr. Joseph A. Ladapo, who was not involved in the vaccine trial, shared his reaction in an exclusive statement to Fox News Digital. (Paul Hennessy/SOPA Images/LightRocket)
"Combining this unsafe product with any vaccine is a mistake, and a disservice to public health."
Amrie Grammer, a Virginia-based immunologist who previously worked with the National Institutes of Health, was not involved in the trial or the vaccine development but commented on the findings.
"Moderna's results from their Ph3 NCT06097273 trial indicate that the dual SARS-CoV-2/influenza immunization is no less effective than two single shots," Grammer told Fox News Digital.
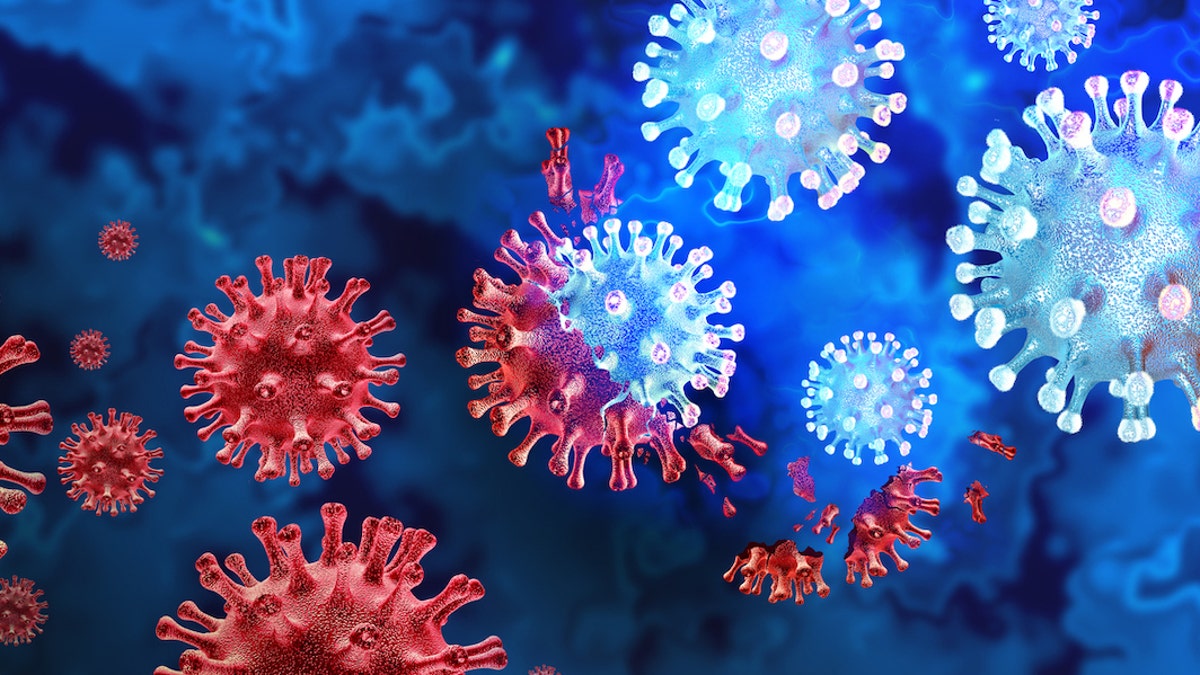
In both groups, mRNA-1083 resulted in "statistically significantly higher immune responses against three influenza virus strains (H1N1, H3N2, and B/Victoria) and against SARS-CoV-2." (iStock)
"This makes it simpler for more Americans to protect themselves from these two serious infections, especially those 65 and older who are most at risk for COVID- and flu- related deaths," she continued.
"Ninety percent of deaths from COVID and 70% to 85% of deaths from the flu in 2023 were in those 65 and older."
"This is especially good news for people who are wary of too many vaccines, even if they believe in them."
Dr. Marc Siegel, clinical professor of medicine at NYU Langone Medical Center and a Fox News medical contributor, was also not involved in the trial but shared insights.
CDC RECOMMENDS ADDITIONAL COVID VACCINE FOR ADULTS 65 AND OVER
"Moderna has been working on combining a vaccine to fight both the latest coronavirus subvariant and the year's flu strain," he told Fox News Digital.
"The phase 3 clinical trials look excellent — safe and effective, with more antibodies made against both than when either immunization is given alone."
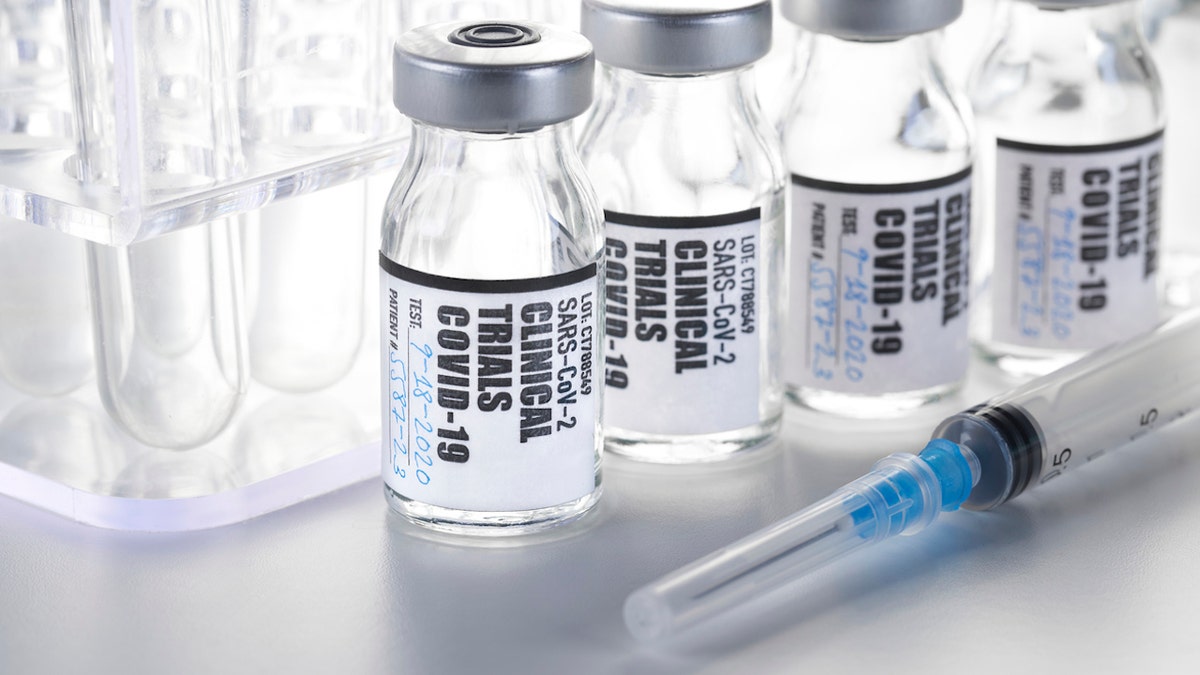
Overall, the experimental vaccine showed an "acceptable tolerability and safety profile," Moderna stated. (iStock)
The effectiveness is likely due to the vaccine "waking up" the immune system to both viruses at the same time, causing a stronger, more varied and more durable response, according to Siegel.
"This is especially good news for people who are wary of too many vaccines, even if they believe in them," he said.
"The most commonly solicited adverse reactions were injection site pain, fatigue, myalgia and headache."
"This shot creates a ‘two-for’ option and should be a useful tool, especially if primary care physicians have ready access to it."
Overall, the experimental vaccine showed an "acceptable tolerability and safety profile," Moderna stated.
CLICK HERE TO SIGN UP FOR OUR HEALTH NEWSLETTER
"The most commonly solicited adverse reactions were injection site pain, fatigue, myalgia and headache," per the release.
As Grammer pointed out, Moderna's phase 3 trial included thousands of people with a "modest adverse event profile, but one can never predict rare adverse events."
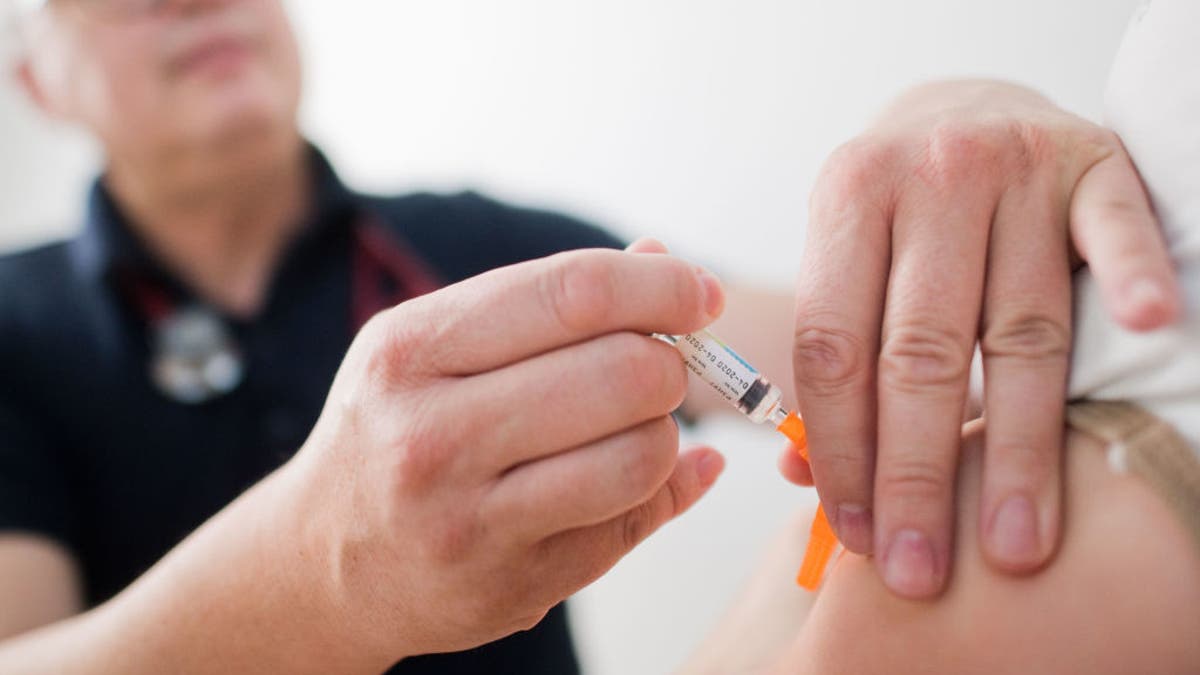
As of May 2022, only some 23% of U.S. adults are up-to-date on COVID vaccines, according to data from the CDC. (Julian Stratenschulte/dpa)
Siegel also chimed in on the vaccine's safety profile.
"Contrary to some public pronouncements, this has been shown to be an overall very safe technology, though it does cause short-term side effects, like sore arm and, rarely, something more pronounced or long-lasting," he told Fox News Digital.
CLICK HERE TO GET THE FOX NEWS APP
As of May 2022, only some 23% of U.S. adults are up-to-date on COVID vaccines, according to data from the Centers for Disease Control and Prevention (CDC).
Flu vaccine coverage for adults was around 47% as of January 2024, per the CDC.
The effectiveness is likely due to the vaccine "waking up" the immune system to both viruses at the same time, a doctor noted. (iStock)
Looking ahead, Moderna plans to present the phase 3 clinical data and submit it for publication.
"Moderna plans to present the Phase 3 clinical data for mRNA-1083 at an upcoming medical conference as well as submit it for publication," the release stated. "The company will engage with regulators on next steps."
For more Health articles, visit www.foxnews/health
Both Novavax and Pfizer-BioNTech also have ongoing clinical trials of SARS-CoV-2/influenza vaccines, Grammer pointed out.
"Our Phase 3 COVID-19-influenza combination study is on track to start in the second half of this year," a spokesperson from Novavax told Fox News Digital.
"A single combination vaccine visit creates a convenience that we believe can translate into improved vaccination rates, especially in older adults, who are most at risk."
Fox News Digital reached out to Pfizer for comment.









































